抗精神病薬の種類と効果について
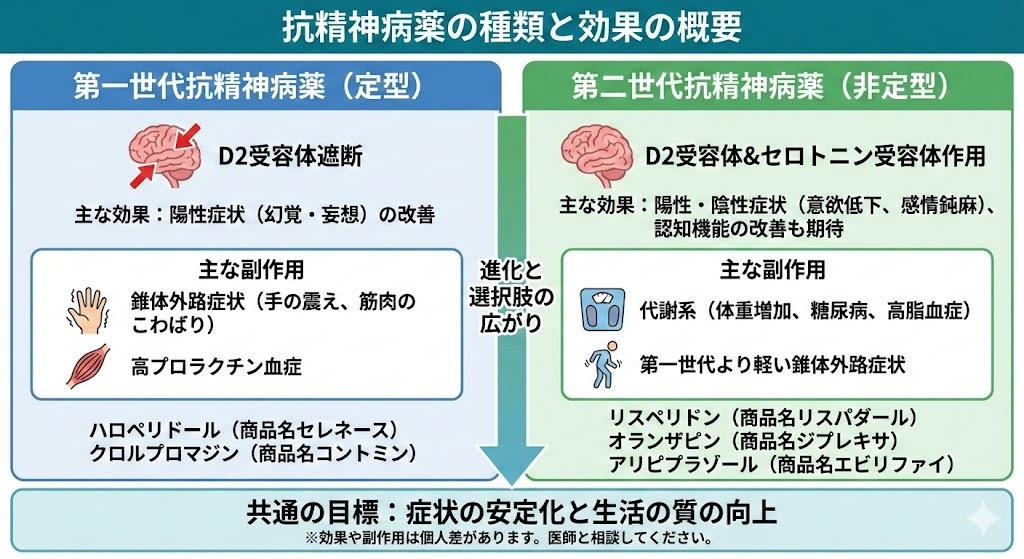
抗精神病薬は統合失調症をはじめとする精神疾患の治療に用いられる重要な薬剤であり、その種類や効果を理解することは臨床現場において非常に重要です。抗精神病薬は大きく分けて「定型抗精神病薬」と「非定型抗精神病薬」の2種類に分類され、それぞれ特徴的な作用機序と効果を持っています。
現在の精神科治療では、副作用プロファイルの良さから非定型抗精神病薬が第一選択薬となることが多くなっていますが、症例によっては定型抗精神病薬が効果的なケースもあります。医療従事者として、これらの薬剤の特徴を把握し、患者さんの状態に応じた最適な薬剤選択ができるようになることが求められています。
抗精神病薬の定型と非定型の分類と特徴

抗精神病薬は、開発された時期や作用機序の違いから「定型抗精神病薬(第一世代)」と「非定型抗精神病薬(第二世代)」に分類されます。それぞれの特徴について詳しく見ていきましょう。
【定型抗精神病薬(第一世代)の特徴】
定型抗精神病薬は、主に強力なドパミンD2受容体遮断作用を持ち、統合失調症の陽性症状(幻覚・妄想など)に対して高い効果を発揮します。しかし、陰性症状(意欲低下など)に対する効果は限定的で、錐体外路症状や高プロラクチン血症などの副作用が出やすいという特徴があります。
定型抗精神病薬は以下の3つのサブタイプに分類されます。
- ブチロフェノン系
特徴:ドパミン遮断作用が強く、陽性症状に対して高い効果を示します。錐体外路症状が出やすいですが、点滴製剤があり急性期の治療に有用です。
- フェノチアジン系
- コントミン/ウィンタミン(クロルプロマジン)
- レボトミン/ヒルナミン(レボメプロマジン)
- フルメジン(フルフェナジン)
- PZC(ペルフェナジン)
- ニューレプチル(プロペリシアジン)
特徴:鎮静作用が強く、不安や興奮状態の改善に効果的です。様々な受容体に作用するため、多岐にわたる副作用が見られることがあります。
- ベンズアミド系
特徴:低用量では抗うつ効果、高用量では抗精神病作用を示します。比較的副作用は少ないものの、高プロラクチン血症が起こりやすいです。
【非定型抗精神病薬(第二世代)の特徴】
非定型抗精神病薬は、ドパミンD2受容体だけでなくセロトニン受容体など複数の受容体に作用し、陽性症状だけでなく陰性症状にも効果を示します。定型抗精神病薬と比較して錐体外路症状などの副作用が少ないことが大きな特徴です。
非定型抗精神病薬は以下の3つに分類されます。
- SDA(セロトニン・ドパミン拮抗薬)
特徴:ドパミンD2受容体とセロトニン5-HT2A受容体の両方に高い親和性を持ち、陽性症状に対して効果的です。定型薬と比べて副作用は少ないものの、錐体外路症状や高プロラクチン血症が見られることがあります。
- MARTA(多元受容体標的化抗精神病薬)
特徴:複数の神経伝達物質受容体に作用し、陽性症状と陰性症状の両方に効果があります。鎮静作用や催眠作用が強い傾向がありますが、体重増加や代謝異常などの副作用リスクがあります。
- DPA/SDAM(ドパミン受容体部分作動薬)
- エビリファイ(アリピプラゾール)
- レキサルティ(ブレクスピプラゾール)
特徴:ドパミン受容体に結合後、弱いシグナルを送る特性を持ち、ドパミンの量を調整します。全体的に副作用が少ないですが、アカシジアが生じることがあり、鎮静作用は比較的弱いです。
抗精神病薬のドパミン受容体への作用機序
抗精神病薬の主要な作用機序は、脳内のドパミン伝達系に対する調節作用です。特に重要なのがドパミンD2受容体への作用であり、これが統合失調症の症状改善に直接関連しています。
【ドパミン仮説と抗精神病薬】
統合失調症のドパミン仮説によれば、脳内の中脳辺縁系におけるドパミン活性の過剰が陽性症状を引き起こし、前頭前野におけるドパミン活性の低下が陰性症状を引き起こすと考えられています。抗精神病薬はこのドパミンバランスを調整することで効果を発揮します。
【定型抗精神病薬のドパミン受容体作用】
定型抗精神病薬は主に中脳辺縁系のドパミンD2受容体を強力に遮断します。これにより陽性症状は改善されますが、同時に線条体のドパミン受容体も遮断されることで、錐体外路症状と呼ばれる副作用(パーキンソン症状、アカシジア、ジストニアなど)が発現します。また、下垂体のドパミン受容体遮断により高プロラクチン血症が引き起こされます。
【非定型抗精神病薬の作用機序の特徴】
非定型抗精神病薬はドパミンD2受容体だけでなく、以下のような複数の受容体にも作用します。
- セロトニン5-HT2A受容体遮断作用。
- 中脳辺縁系でのドパミン遊離を促進し、陰性症状の改善に寄与
- 線条体でのドパミン遊離を促進し、錐体外路症状を軽減
- ドパミン受容体への部分作動作用。
- DPA系薬剤(アリピプラゾールなど)では、ドパミンの量が多い部位では拮抗薬として、少ない部位では作動薬として働く
- これにより、ドパミン活性を「安定化」する効果がある
- 受容体占有率と効果の関係。
- D2受容体占有率が60-70%で治療効果が現れ始める
- 占有率が80%を超えると錐体外路症状などの副作用リスクが高まる
- 非定型抗精神病薬はこの「治療ウィンドウ」内で作用することが多い
- 受容体からの解離速度。
- 非定型抗精神病薬はD2受容体からの解離が速い(fast off)特性を持つ
- これにより、内因性ドパミンと競合せず、生理的なドパミン機能を維持
これらの複合的な作用機序により、非定型抗精神病薬は定型抗精神病薬と比較して、より広範囲の症状に効果を示しながら、副作用を軽減することが可能となっています。
抗精神病薬の副作用と対策について
抗精神病薬の副作用は、患者さんのQOLを大きく左右し、服薬継続性にも影響を与える重要な要素です。主な副作用とその対策について理解しておくことは、適切な薬剤管理において不可欠です。
【主な副作用】
- 錐体外路症状(EPS)
- パーキンソン症状:筋強剛、振戦、動作緩慢
- アカシジア:静座不能、常に動いていたい感覚
- ジストニア:筋肉の持続的収縮による異常姿勢
- 遅発性ジスキネジア:口唇や顔面の不随意運動
対策:抗コリン薬の併用(ビペリデン、トリヘキシフェニジルなど)、β遮断薬の使用(アカシジアに対して)、可能であれば原因薬剤の減量または変更
- 自律神経系副作用
対策:徐々に増量する、分割投与、十分な水分摂取の促進、必要に応じて対症療法薬の併用
- 内分泌・代謝系副作用
対策:定期的な血液検査によるモニタリング、栄養指導、運動促進、必要に応じて薬剤変更
- 心血管系副作用
- QT延長:致死的不整脈のリスク
- 心筋炎:クロザピンでのリスク
対策:定期的な心電図検査、電解質バランスの維持、ほかのQT延長薬との併用回避
- 血液学的副作用
- 顆粒球減少症:クロザピンで特に注意が必要
対策:定期的な血球数モニタリング、感染徴候の観察
【副作用と薬剤選択】
薬剤選択においては、患者さんの症状だけでなく、想定される副作用と患者特性を考慮する必要があります。
- 若年患者:体重増加、代謝異常のリスクが高いため、アリピプラゾールなどDPA系が比較的安全
- 高齢者:錐体外路症状、認知機能低下、心血管リスクが高いため、低用量から開始し慎重な調整が必要
- 身体疾患合併患者:合併症に応じた薬剤選択(心疾患患者にはQT延長の少ないものを選択するなど)
【副作用モニタリングの重要性】
定期的な副作用モニタリングは、早期発見と対応のために不可欠です。
- 投与開始時:ベースライン評価(体重、血圧、心電図、血液検査など)
- 定期的なフォロー:体重測定、血圧測定、錐体外路症状の評価
- 半年~1年ごと:代謝パラメータ(血糖、脂質プロファイルなど)、心電図検査
適切なモニタリングと副作用対策を行うことで、患者さんのQOL向上と治療継続率の改善につながります。
抗精神病薬の使い分けと個別化治療
抗精神病薬の種類と効果を理解したうえで、個々の患者さんに最適な薬剤を選択することは臨床的に重要です。抗精神病薬の使い分けには、症状プロファイル、既往歴、副作用リスク、患者さんの希望などを総合的に考慮する必要があります。
【症状による使い分け】
- 陽性症状優位の場合
- リスペリドン、ブロナンセリン(SDA系)などが効果的
- 定型抗精神病薬も考慮(特に急性期の興奮状態にはハロペリドールの注射など)
- 陰性症状優位の場合
- オランザピン(MARTA系)、アリピプラゾール(DPA系)などが有効
- 陰性症状にはMARTA系が特に効果的とされる
- 認知機能障害への配慮
- 抗コリン作用の少ないアリピプラゾール、ブレクスピプラゾールが望ましい
- 高齢者の場合、抗コリン作用の強い薬剤は認知機能をさらに低下させる可能性
- 睡眠障害を伴う場合
- クエチアピン、オランザピンなど鎮静作用の強い薬剤が適している
- 不眠が主訴の場合、就寝前の服用を検討
【身体状態による使い分け】
- 代謝リスクが高い患者
- 糖尿病や肥満のリスクがある場合:アリピプラゾール、ブレクスピプラゾールなどが望ましい
- オランザピン、クエチアピンは代謝への影響が大きいため注意
- 心血管疾患がある場合
- QT延長リスクの少ないルラシドンやアリピプラゾールが望ましい
- 起立性低血圧リスクの少ない薬剤を選択
- 高プロラクチン血症の懸念
- 生殖年齢の女性:アリピプラゾール、クエチアピンなどが望ましい
- リスペリドン、パリペリドン、定型抗精神病薬はプロラクチン上昇作用が強い
【治療抵抗性への対応】
- クロザピンの位置づけ
- 2種類以上の抗精神病薬に反応しない治療抵抗性統合失調症には、クロザピンが唯一エビデンスのある選択肢
- 無顆粒球症のリスクがあるため、厳重な血液モニタリングが必須
- 持効性注射剤(LAI)の活用
【個別化治療のアプローチ】
抗精神病薬の個別化治療には、以下のような段階的アプローチが有効です。
- 患者の症状プロファイル、身体状態、嗜好を総合的に評価
- 薬剤特性と患者プロファイルのマッチングを検討
- 低用量から開始し、効果と副作用を慎重にモニタリングしながら調整
- 効果不十分または副作用が著しい場合は薬剤変更を検討
- 必要に応じて薬剤併用を考慮(ただし、根拠に基づいた併用を心がける)
適切な使い分けと個別化治療により、患者さんのQOLを最大化しながら、症状の改善と副作用の最小化を図ることが可能になります。
抗精神病薬の新世代製剤と今後の展望
抗精神病薬の開発は現在も進行中であり、より効果的で副作用の少ない新世代の製剤が登場しています。これらの新薬と今後の展望について理解することは、最新の精神科薬物療法を実践するために重要です。
【第三世代抗精神病薬の特徴】
現在、アリピプラゾールやブレクスピプラゾールなどのドパミン部分作動薬は「第三世代抗精神病薬」と呼ばれることがあります。これらの薬剤は以下の特徴を持ちます。
- ドパミン安定化作用
- ドパミンが過剰な部位では拮抗薬として
- ドパミンが不足している部位では作動薬として機能
- これにより陽性症状と陰性症状の両方に効果を発揮
- 受容体選択性の向上
- より特定の受容体サブタイプに選択的に作用
- 不要な受容体作用による副作用を軽減
- 副作用プロファイルの改善
- 代謝系副作用が少ない
- 高プロラクチン血症のリスクが低い
- 認知機能への悪影響が少ない
【新しい投与形態と製剤】
- 持効性注射剤(LAI)の進化
- より長期間作用する製剤(3ヶ月製剤など)
- 注射部位反応の少ない製剤
- 自己注射可能な製剤の開発
- 経口崩壊錠(OD錠)の普及
- 水なしでも服用可能
- アドヒアランス向上に寄与
- 嚥下困難な患者にも使用しやすい
- 経皮吸収システム
【精密医療に向けた取り組み】
- 薬理遺伝学(ファーマコゲノミクス)の応用
- CYP酵素多型に基づく投与量調整
- 薬物応答性の予測マーカーの開発
- 副作用リスクの個別化予測
例えば、CYP2D6やCYP1A2などの代謝酵素の遺伝的変異は、抗精神病薬の効果や副作用に影響することが明らかになっています。これらの遺伝情報を活用した治療選択が将来的に標準となる可能性があります。
- バイオマーカーを用いた治療反応性の予測
- 脳画像所見(D2受容体占有率など)
- 血中バイオマーカー(炎症マーカーなど)
- 神経生理学的マーカー(事象関連電位など)
【今後の研究方向性】
- 新しい作用機序を持つ抗精神病薬
- グルタミン酸系調節薬
- GABA系調節薬
- 神経炎症調節薬
- 治療抵抗性症例に対する新たなアプローチ
- クロザピン以外の選択肢の開発
- 補助療法としての新規薬剤(抗炎症薬など)
- 非薬物療法との最適な組み合わせ
- 認知機能や社会機能の改善を目指した薬剤開発
- 現状の抗精神病薬は陽性症状には効果的だが、認知機能や社会機能の改善には限界がある
- これらの領域を特異的に改善する薬剤の開発が進行中
【実践への応用】
新世代の抗精神病薬を臨床で活用する際には、以下の点に注意が必要です。
- 新薬のエビデンスと適応を正確に理解する
- コスト面も考慮した薬剤選択
- 長期的な安全性データが限られている場合があることを念頭に置く
- 個々の患者特性に合わせた選択
抗精神病薬の進化は、統合失調症をはじめとする精神疾患の治療に新たな選択肢をもたらしています。これらの新しい治療オプションを理解し適切に活用することで、患者さんのリカバリーと社会復帰をより効果的に支援することが可能になるでしょう。
精神科薬物治療の未来は、より個別化され、効果的で、副作用の少ない治療法の開発に向かっています。医療従事者として、常に最新のエビデンスを学び続け、患者さんにとって最適な治療を提供することが重要です。
【指定第2類医薬品】パブロン鼻炎カプセルSα 48カプセル