ギラン・バレー症候群診療ガイドライン2024における最新知見
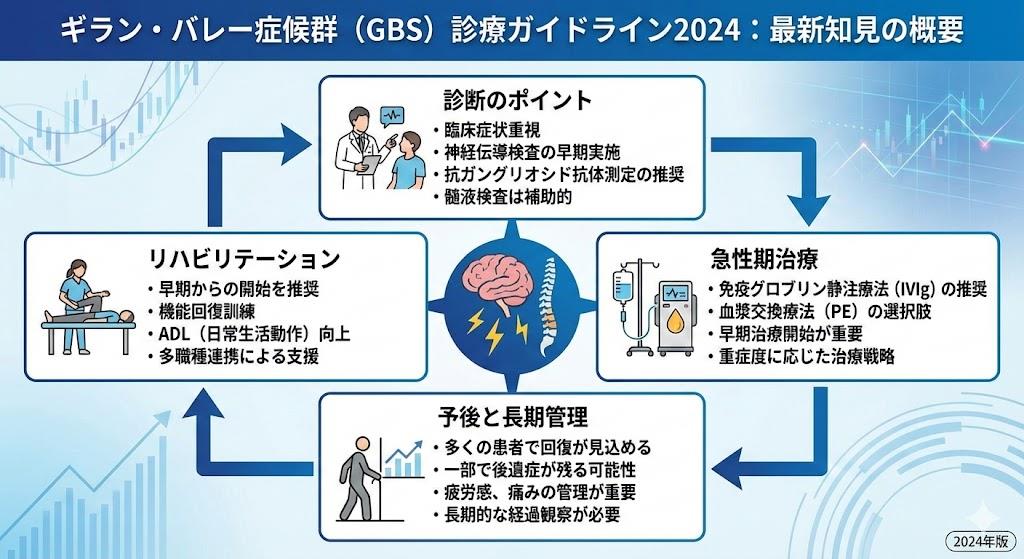
ギラン・バレー症候群の診断基準と検査方法

ギラン・バレー症候群の診断は、主に臨床症候に基づいて行われ、2024年版ガイドラインではより明確な診断基準が示されています 。診断に必要な特徴として、2肢以上の進行性の筋力低下が挙げられ、その程度は軽微な両下肢の筋力低下から四肢、体幹、球麻痺、顔面神経麻痺、外転神経麻痺を含む完全麻痺まで様々です 。
参考)https://www.neurology-jp.org/guidelinem/pdf/gbs_2024_01.pdf
診断を支持する重要な検査として、脳脊髄液検査では蛋白細胞解離が特徴的とされています 。脳脊髄液内の蛋白が増加し、細胞数(白血球数)は正常という変化がみられることが多く、これは診断の根拠となります 。一方で、この所見がみられないこともあるため、診断に必須ではないとされています 。
参考)ギラン・バレー症候群
電気生理学的検査では、運動神経伝導速度の低下や伝導ブロックなどがみられ、特徴的な波形によりAIDP(急性炎症性脱髄性多発ニューロパチー)とAMAN(急性運動軸索型ニューロパチー)を判別することができます 。血液検査では、抗ガングリオシド抗体の検出が行われ、約60%の患者でこれらの抗体が確認されます 。
参考)https://www.s-ahs.org/jahs/JAHS%20Vol11(2)%20013.pdf
ギラン・バレー症候群におけるHughes機能評価スケール
ギラン・バレー症候群の重症度評価には、Hughes機能グレード尺度が広く用いられています 。このスケールは0から5まで6段階に分かれており、Grade 0が正常、Grade 1が軽微な神経症候があるが走行可能、Grade 2が補助なしで10メートル歩行可能、Grade 3が補助または支持により10メートル歩行可能、Grade 4がベッドまたは車椅子に限定、Grade 5が補助換気を必要とする状態として分類されています 。
参考)https://www.neurology-jp.org/guidelinem/gbs/sinkei_gbs_2013_01.pdf
このスケールは治療効果の判定や予後予測にも重要な役割を果たしています 。研究によると、入院時のHughes機能グレード尺度が予後に大きく影響し、Grade 3以上の重症例では退院時の機能予後が不良となるリスクが高いことが報告されています 。
参考)https://pmc.ncbi.nlm.nih.gov/articles/PMC10040339/
また、機械的人工呼吸が必要となるGrade 5の患者では、死亡率との関連が強く、早期の重症度評価が治療戦略の決定において極めて重要となります 。このため、診療現場では入院時の迅速なHughes評価が推奨されています 。
参考)https://pmc.ncbi.nlm.nih.gov/articles/PMC4576316/
ギラン・バレー症候群における免疫グロブリン療法と血漿交換療法
2024年版ガイドラインでは、免疫グロブリン静注療法(IVIg)と血漿浄化療法(主に単純血漿交換法:PE)のいずれも、発症早期から治療を開始すれば有効な治療法であることが明記されています 。これらの治療法は同等の効果があるとされており、多くの臨床試験でその有効性が確認されています 。
参考)https://www.neurology-jp.org/guidelinem/gbs/sinkei_gbs_2013_05.pdf
IVIgは400mg/kg/日×5日間の投与が標準的な治療法として推奨されており、患者に免疫グロブリンを投与することで免疫反応を調節します 。一方、血漿交換療法は血液から有害な抗体を除去する方法で、特に腎機能障害を合併する症例では血漿交換の方が効果的であるとする報告もあります 。
参考)https://www.jstage.jst.go.jp/article/jsdt/42/5/42_5_403/_pdf
血漿浄化療法については、単純血漿交換(PE)に関するエビデンスが二重膜濾過血漿交換などよりも高いことが強調され、PEの実施が推奨される形となりました 。治療選択に際しては、患者の全身状態や合併症を考慮して個別に決定することが重要です 。
参考)https://www.jsnt.gr.jp/guideline/img/meneki_4.pdf
ギラン・バレー症候群に対するリハビリテーション療法の役割
ギラン・バレー症候群のリハビリテーションは、急性期から生活期に至るまで包括的に行う必要があります 。リハビリテーションの目的は、低下した身体機能の回復を促し、日常生活への復帰をスムーズにすることです 。
参考)ギラン・バレー症候群って何?医師が解説
急性期の初期段階では、関節の拘縮を防ぐための関節可動域訓練や寝たきり状態を防ぐための体位変換が中心となります 。筋は低緊張状態であり、急激な過度の伸張が加わると筋断裂を生じやすいため、ストレッチを行う際には愛護的に行うことが重要です 。
参考)ギラン・バレー症候群のリハビリテーション方法-リニューロ・川…
症状が軽快してくると、筋力トレーニングや歩行訓練、日常生活動作訓練など、より積極的な運動療法が開始されます 。ただし、ギラン・バレー症候群や脱髄疾患といった末梢神経障害では、患者が筋力増強訓練をやりすぎると、逆に筋力が低下してしまう現象が報告されているため注意が必要です 。装具療法も重要な要素で、下肢の筋力低下が強い場合には長下肢装具を使用し、回復に応じて段階的に短下肢装具へと変更していきます 。
ギラン・バレー症候群における新規治療法と今後の展望
2024年版ガイドラインでは、従来の治療法に加えて新規治療法についても言及されています 。特に注目されているのが補体阻害療法の可能性で、IVIg単独療法に対して補体阻害薬エクリズマブ併用の有効性が検討されています 。第Ⅱ相試験では、併用群で機能回復が早いとの結果が得られており、今後の臨床応用が期待されています。
参考)https://for-professionals.neuroimmunology.jp/img/highlights/conference36/36_sym_5.pdf?v=20250725
また、免疫関連有害事象(irAE)として発症するギラン・バレー症候群が増加しており、これに対してはステロイドが有効との症例報告が複数みられています 。新ガイドラインでは、irAE-GBSに対するステロイドの使用については否定しない立場をとるに至りました。
一方で、IVIgとステロイドの併用については「積極的には推奨しない」との方針も示されています 。このような治療選択の細分化は、個々の患者の病態に応じたより精密な治療戦略の構築を可能にしています。
抗補体薬や免疫グロブリン皮下注射などの新規薬物療法の開発も進んでおり 、今後さらなる臨床研究の進展により、ギラン・バレー症候群治療の選択肢が広がることが期待されます 。これらの新しい治療オプションは、従来の治療に抵抗性を示す症例や特殊な病型に対する有効な治療手段となる可能性があります。
参考)https://www.jstage.jst.go.jp/article/jjrmc/60/3/60_60.192/_pdf
[指定医薬部外品] 大正製薬 新ビオフェルミンS錠 550錠 61日分整腸剤【Amazon.co.jp限定】 [乳酸菌/ビフィズス菌/フェーカリス菌/アシドフィルス菌 配合] 腸内フローラ改善 便秘や軟便に