アスペルギルス症ガイドライン診断治療
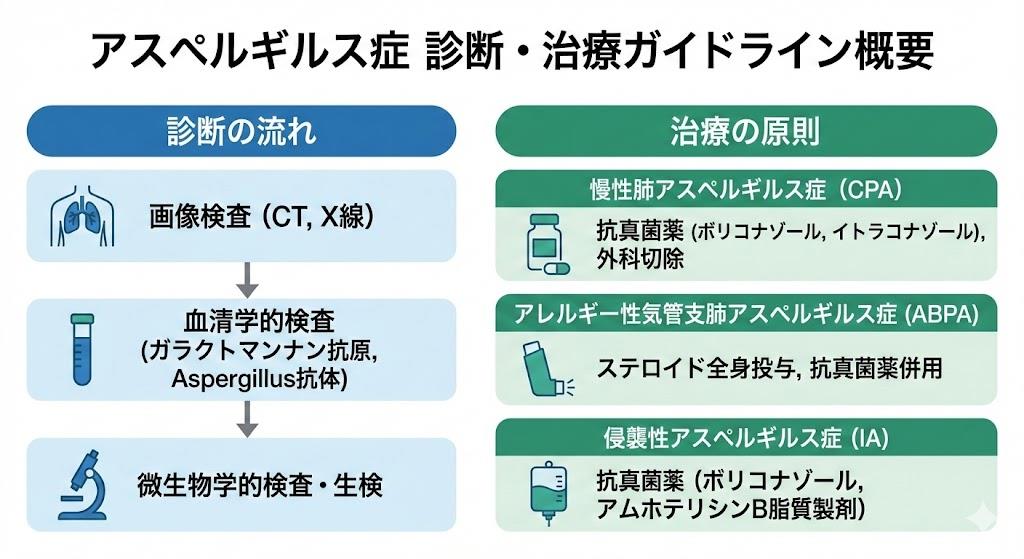
アスペルギルス症診断基準最新改訂内容

アスペルギルス症の診断基準は、国際的にEORTC/MSG(European Organization for Research and Treatment of Cancer/Mycoses Study Group)基準が広く採用されています。この基準では、診断の確実性に応じて3つのカテゴリーに分類されています。
参考)http://www.kankyokansen.org/uploads/uploads/files/jsipc/20191115-iryo-seminar_3.pdf
Proven(確定診断例) では、無菌検体の病理・細胞組織学的検査でAspergillus菌を確認するか、無菌検体からAspergillusが発育することが必要です。Probable(臨床診断例) は、宿主因子・臨床的基準・微生物学的基準の3つを全て満たす必要があります。
2024年には、ISHAM(国際医真菌学会)がアレルギー性気管支肺アスペルギルス症(ABPA)の新しいコンセンサス基準を発表。従来の診断基準では感度が低い問題がありましたが、日本のAsanoらが提唱した診断基準では特異度90%を維持しつつ感度94-96%という極めて高い精度を実現しています。
参考)https://hokuto.app/calculator/tDiIvKmrklvstMwcejQn
画像診断では、胸部CTにおけるhalo sign(ハロー徴候)、air crescent sign、空洞、楔状の肺区域性・肺葉性浸潤影が重要な所見です。好中球減少患者では胸部単純X線で早期病変を検出できないため、胸部CT検査が必須となります。
参考)https://www.jstct.or.jp/uploads/files/guideline/01_04_shinkin02.pdf
アスペルギルス症治療ガイドライン薬剤選択
本邦の深在性真菌症ガイドライン2014年版では、侵襲性アスペルギルス症の第一選択薬として**ボリコナゾール(VRCZ)とミカファンギン(MCFG)**が推奨されています。
参考)https://www.kameda.com/pr/pulmonary_medicine/cppachronic_progressive_pulmon.html
国際的には、ボリコナゾールまたはイサブコナゾールが第一選択とされており、イサブコナゾールはボリコナゾールと同等の効力を有しながら副作用がより少ないという特徴があります。重症例ではリポソーマル・アムホテリシンBが代替薬として使用されます。
参考)https://www.msdmanuals.com/ja-jp/professional/13-%E6%84%9F%E6%9F%93%E6%80%A7%E7%96%BE%E6%82%A3/%E7%9C%9F%E8%8F%8C/%E3%82%A2%E3%82%B9%E3%83%9A%E3%83%AB%E3%82%AE%E3%83%AB%E3%82%B9%E7%97%87
慢性進行性肺アスペルギルス症(CPPA)の治療では、初期治療として全身状態不良な場合は入院で2週間以上の静注治療を行います。ファンガード®(ミカファンギン)150-300mg/日またはブイフェンド®(ボリコナゾール)の点滴静注が標準的です。
維持療法では経口薬による6ヶ月以上の長期投与が必要で、病状が安定すれば中止を検討します。治療期間は症例によっては年単位に及ぶこともあり、外来での継続治療が重要となります。
参考)https://www.jstage.jst.go.jp/article/kansenshogakuzasshi/97/3/97_r23001/_pdf
深在性真菌症ガイドライン2014年版の診療指針に関する詳細情報
アスペルギルス症血清学的検査診断法
血清診断法は侵襲的検査が困難な免疫不全患者において重要な役割を果たします。現在臨床で使用される主要な検査法には以下があります。
参考)http://journal.kansensho.or.jp/Disp?pdf=0780070566.pdf
ガラクトマンナン抗原検査は、アスペルギルスが産生する特異的抗原を検出する方法で、血清および気管支肺胞洗浄液(BAL)で測定可能です。この検査は感染の有無や病状の進行度を評価するのに有効で、特に侵襲性アスペルギルス症の診断において重要です。
参考)https://www.sms.co.jp/colum/aspergillus-antigens/
β-グルカン測定は、真菌細胞壁の主要構成成分を検出する非特異的な検査ですが、早期診断の補助として活用されています。測定方法には、カイネティック比色法によるファンギテック G テスト MKと比濁時間分析法があります。
Lateral Flow Device (LFD) testは迅速診断法として注目されており、検査結果を短時間で得ることができます。これらの血清学的検査を組み合わせることで、診断精度の向上が期待できます。
分子生物学的検査ではPCR法による遺伝子診断も実用化されており、培養検査の補完的役割を担っています。
アスペルギルス症薬剤耐性対策
近年、アゾール系抗真菌薬に対する耐性アスペルギルスの検出が世界的に問題となっています。耐性機序として、cyp51Aによってコードされる14-alpha-demethylase(CYP51)の変異による標的部位への親和性低下が主要な原因です。
参考)https://www.chemotherapy.or.jp/journal/jjc/06102/061020149.pdf
薬剤耐性の発生機序には、標的部位の変異、標的部位の過剰発現、排出ポンプの活性化などが関与しています。特にcyp51A遺伝子のホットスポットでの変異が耐性化の主因となっており、イトラコナゾール(ITCZ)を含む各種アゾール系薬剤に対する耐性パターンが報告されています。
耐性対策として、感受性検査の実施と適切な薬剤選択が重要です。アゾール系薬剤が使用できない場合は、アムホテリシンBリポソーム製剤の間欠投与による外来治療や、抗真菌薬の併用療法が検討されます。
慢性肺アスペルギルス症では、血流の存在しない空洞内に病原体が存在するため治療効果が得られにくく、薬剤耐性や副作用により外来診療が困難になる場合があります。このような難治例では、多剤併用療法や新規抗真菌薬の使用が必要となります。
予防的投与も重要な戦略で、高リスク患者(移植片対宿主病患者、急性骨髄性白血病による好中球減少患者)にはポサコナゾールまたはイトラコナゾールの予防投与が推奨されています。
アスペルギルス症重症患者管理戦略
ICU重症患者における侵襲性肺アスペルギルス症(IPA)は特に予後不良で、迅速な診断と適切な治療が生命予後を左右します。2025年に発表されたドイツのガイドラインでは、重症患者に特化した管理戦略が提示されています。
参考)https://www.kameda.com/depts/kei_nakashima/entry/04306.html
診断アプローチでは、適応がある場合は侵襲性アスペルギルス症を積極的に考慮し、適切な診断検査を迅速に開始することが重要です。画像診断では、急性経過の結節影、楔状浸潤影を呈するため、肺接合菌症、細菌性肺炎、血液悪性腫瘍の肺浸潤、移植片対宿主病との鑑別が必要です。
参考)https://hokuto.app/post/m20I3MSZswGNFdYIpuLJ
治療選択において、第一選択治療としてイサブコナゾールとボリコナゾールが推奨され、代替薬としてリポソーマル・アムホテリシンBが位置づけられています。治療期間は6-12週間が一般的ですが、重症例では2-4週間の集中治療が必要な場合もあります。
参考)https://kobe-kishida-clinic.com/respiratory-system/respiratory-disease/pulmonary-aspergillosis/
免疫抑制状態の改善が完全な治癒には不可欠で、好中球減少の回復やコルチコステロイドの中止が重要な要素となります。好中球減少が再発すれば再燃の頻度が高くなるため、基礎疾患の管理も並行して行う必要があります。
モニタリングでは、症状や画像所見の改善を確認しながら治療を継続し、血清学的マーカーの推移を参考にして治療効果を評価します。外来治療への移行時期の判断も重要で、経口薬による長期維持療法への切り替えを適切に行うことが求められます。
ICU重症患者における侵襲性肺アスペルギルス症の最新ガイドライン
【指定第2類医薬品】イブA錠 90錠