核酸アナログ製剤の種類と一覧について
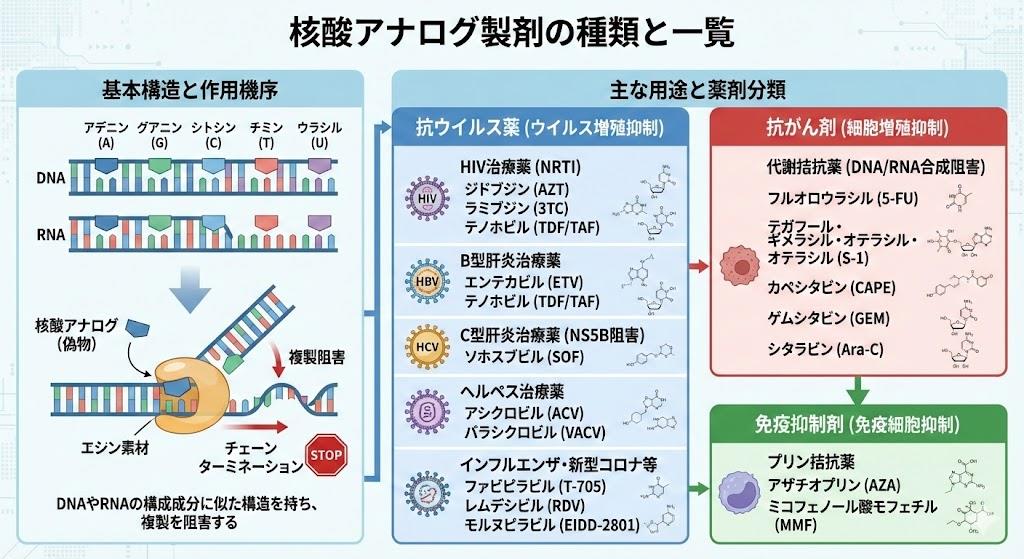
核酸アナログ製剤とは:作用機序と特徴

核酸アナログ製剤は、B型肝炎ウイルス(HBV)に対する治療薬として重要な役割を果たしています。これらの薬剤は、ウイルスの増殖に必要なDNA合成を阻害することで効果を発揮します。
核酸アナログ製剤の作用機序は、DNA(デオキシリボ核酸)を構成する核酸塩基(アデニン、グアニン、チミン、シトシン)の類似物質として機能することにあります。これらの薬剤がB型肝炎ウイルスの逆転写酵素によってウイルスDNAに取り込まれると、DNA鎖の伸長が停止し、ウイルスの複製が阻害されるのです。
特筆すべき点として、これらの製剤は人間の細胞が持つDNAポリメラーゼではあまり認識されず、主にウイルスの酵素に特異的に作用するため、理論上は人間のDNAへの影響が最小限に抑えられています。ウイルスの逆転写酵素は天然型でない核酸も取り込む性質があり、むしろ天然でない方を多く取り込むという特性があるのです。
核酸アナログ製剤の最大の特徴は以下の点にあります。
- ウイルス増殖を直接抑制する効果が高い
- 経口投与が可能で外来治療に適している
- インターフェロンと比較して副作用が少ない
- 年齢や肝機能に関わらず広く使用可能
ただし重要な注意点として、これらの薬剤はB型肝炎を「完治」させるものではなく、あくまでウイルスの増殖を抑制して肝炎を鎮静化させることが目的です。そのため、日本肝臓学会のB型肝炎治療ガイドラインでも、治療目標は「HBV感染者の生命予後およびQOLを改善すること」と定められています。
核酸アナログ製剤の種類:5種類の薬剤一覧と比較
日本で承認されているB型肝炎治療用の核酸アナログ製剤は、現在5種類あります。それぞれの特徴や発売年、メーカー情報を含めて一覧で紹介します。
| 一般名(略号) | 商品名 | 発売年 | メーカー | 特徴 |
|---|---|---|---|---|
| ラミブジン(LAM) | ゼフィックス | 2000年 | GSK | シトシンのアナログ、最初に承認された核酸アナログ製剤[2] |
| アデホビルピボキシル(ADV) | ヘプセラ | 2004年 | GSK | アデニンのアナログ、2022年5月販売中止[2][8] |
| エンテカビル水和物(ETV) | バラクルード | 2006年 | ブリストル | グアニンのアナログ、現在の第一選択薬[2][5] |
| テノホビル ジソプロキシルフマル酸塩(TDF) | テノゼット | 2014年 | GSK | 元々HIV治療薬、催奇形性が低い[7] |
| テノホビル アラフェナミドフマル酸塩(TAF) | ベムリディ | 2017年 | ギリアド | TDFより肝臓移行性が効率的、腎・骨への影響が少ない[6][7] |
これらの薬剤の中で、現在B型肝炎治療の第一選択薬として推奨されているのは、エンテカビル(ETV)、テノホビル ジソプロキシルフマル酸塩(TDF)、テノホビル アラフェナミドフマル酸塩(TAF)の3種類です。これらは強力な抗ウイルス作用と低い耐性出現率を特徴としています。
特に注目すべきは最新の薬剤であるテノホビル アラフェナミドフマル酸塩(TAF)です。この薬剤は、TDFの改良版として開発され、肝臓への移行性が向上しており、より低用量で同等の効果を発揮します。また、腎機能低下や骨密度低下などの副作用リスクが低減されている点も大きな利点です。
核酸アナログ製剤の選択においては、患者の年齢、肝機能、腎機能、骨密度状態、妊娠の可能性などを総合的に考慮して、最適な薬剤を選択することが重要です。
核酸アナログ製剤の副作用と長期使用時の注意点
核酸アナログ製剤はインターフェロン療法と比較して副作用が少ないとされていますが、長期間の使用においていくつかの注意すべき副作用が報告されています。各薬剤の主な副作用と長期使用時の注意点について解説します。
【核酸アナログ製剤の一般的な副作用】
核酸アナログ製剤は基本的に忍容性が高く、多くの患者さんがこれらの薬剤を問題なく服用できますが、製剤によって特有の副作用に注意が必要です。
【薬剤別の特徴的な副作用】
- エンテカビル(バラクルード)
- 鼻咽頭炎
- 倦怠感
- 頭痛
- 催奇形性:妊娠中や妊娠の可能性がある女性には投与できません
- テノホビル ジソプロキシルフマル酸塩(テノゼット)
- 腎機能低下:クレアチニン上昇や糸球体濾過量(GFR)の低下
- 低リン血症
- 骨密度低下:長期使用による骨折リスク増加の可能性
- 妊娠への影響:比較的安全とされており、一部の地域では妊娠後期での使用例も報告されています
- テノホビル アラフェナミドフマル酸塩(ベムリディ)
- テノゼットと比較して腎機能や骨密度への影響が少ない
- 比較的新しい薬剤のため、長期的な安全性データはまだ蓄積中です
【長期使用時の注意点】
核酸アナログ製剤を長期間使用する際には、以下の点に注意が必要です。
- 定期的な腎機能検査
特にテノホビル系薬剤(TDFやTAF)使用時は、尿検査や血液検査による腎機能のモニタリングが重要です。腎機能に異常が見られた場合は、薬剤の変更が検討されます。
- 骨密度のモニタリング
長期のテノホビル系薬剤の使用では、骨密度低下のリスクがあるため、定期的な骨密度測定が推奨されます。
- 薬剤耐性の監視
定期的なウイルス量測定により、耐性ウイルスの出現を早期に発見することが大切です。特にラミブジンなど耐性出現率の高い薬剤では重要です。
- 妊娠・出産に関する注意
妊娠希望の女性に対しては、催奇形性のリスクが低いとされるテノホビル系の薬剤が選択されることが多いです。
長期間の核酸アナログ製剤の使用においては、これらの副作用のリスクと肝炎鎮静化による利益のバランスを考慮することが重要です。副作用の早期発見と適切な対応により、長期的な安全性を確保することが可能です。
核酸アナログ製剤の耐性ウイルス出現とその対策
核酸アナログ製剤の長期使用における最大の課題の一つが、薬剤耐性ウイルスの出現です。B型肝炎ウイルス(HBV)は複製の過程で変異を起こしやすく、薬剤の継続使用により耐性変異株が選択的に増殖することがあります。各薬剤の耐性ウイルス出現率とその対策について詳しく見ていきましょう。
【薬剤別の耐性ウイルス出現率】
- ラミブジン(ゼフィックス)
- 1年で約20%
- 3年で約50%
- 長期投与で高率に耐性ウイルスが出現するため、現在は第一選択薬ではありません
- アデホビル(ヘプセラ)
- 高用量での腎障害の副作用のため、常用量が低く設定され抗ウイルス力が弱い
- 主にラミブジン耐性例に使用されていましたが、現在は販売中止
- エンテカビル(バラクルード)
- 核酸アナログ製剤未使用患者に対する3年間の投与で耐性ウイルスの出現率は2~3%と低率
- ラミブジン耐性例では耐性出現率が上昇します
- テノホビル(テノゼット/ベムリディ)
- 長期観察でも耐性ウイルス出現は確認されていない
- 現在の最も耐性バリアの高い薬剤の一つです
【耐性ウイルス出現時の対応策】
- ラミブジン耐性ウイルス
- テノホビル(TDFまたはTAF)への切り替えが最も効果的
- これらの薬剤はラミブジン耐性ウイルスに対しても交差耐性がありません
- アデホビル耐性ウイルス
- テノホビルへの切り替えが推奨される
- アデホビル二重耐性の場合は、効果が減弱することがあります
- エンテカビル耐性ウイルス
- テノホビルへの切り替えが推奨される
- 多剤耐性の場合は、テノホビル + エンテカビルの併用療法も検討されます
【耐性ウイルス出現を防ぐための戦略】
- 初回治療での最適な薬剤選択
- 現在の第一選択薬は、耐性バリアの高いエンテカビル、テノホビルTDF、テノホビルTAF
- ラミブジンなど耐性出現率の高い薬剤は新規治療では推奨されません
- 定期的なウイルス量モニタリング
- 治療開始後の定期的なHBV DNA量測定により、耐性ウイルスの出現を早期に発見することが重要です
- ウイルス量が再上昇した場合は耐性発現を疑います
- アドヒアランスの維持
- 服薬の遵守率が低いと、不十分な薬剤濃度により耐性ウイルスが選択されやすくなります
- 患者教育と定期的なフォローアップが重要です
核酸アナログ製剤の耐性問題は、B型肝炎治療の長期的な課題ですが、現在の第一選択薬は耐性バリアが高く、適切な管理下では多くの患者で長期的なウイルス抑制が期待できます。
核酸アナログ製剤を用いた治療戦略と今後の展望
B型肝炎治療における核酸アナログ製剤の使用は、日本肝臓学会の治療ガイドラインに基づいて体系化されています。また、近年では新たな治療アプローチも研究されています。
【治療対象と薬剤選択】
核酸アナログ製剤による治療を開始する基準は、主にHBV DNA陽性かつALT値の上昇(31 IU/L以上)が持続する場合です。肝硬変患者ではHBV DNA陽性であれば、ALT値に関わらず治療適応となります。
年齢による治療選択も重要です。
- 35歳未満:免疫応答によるセロコンバージョンが期待され、インターフェロン治療が選択されることが多い
- 35歳以上:セロコンバージョンの可能性が低く、核酸アナログ療法によるウイルス抑制治療が選択される
現在、核酸アナログ製剤未使用例への第一選択薬としては、ETV、TDF、TA
【指定第2類医薬品】パブロン鼻炎カプセルSα 48カプセル